新薬の供給に介入する
政府が新薬の供給に間接的に介入する方法として以下の方法があります。
①基礎研究の支援
②製薬会社に対する税制優遇
③市場独占の法的容認
④ジェネリック医薬品の参入
⑤バイオシミラーについての扱い
⑥政策(医薬品の値段や臨床試験の基準の制定)
この中でも、Royalty Pharma に直接かかわってくるのは③、④、⑤、⑥ですが、特に大事なのは③市場独占の法的容認と、⑤バイオシミラーについての扱いでしょうか。
基礎研究の支援
政府は大学の研究室などで行われる基礎研究に対して資金を提供することで、結果的に新薬の研究を促します。基礎研究が行われ、その研究結果を各企業が使用することで研究開発費を抑えることができます。また、基礎研究を行うことで、病気のメカニズムに関して新しい発見をすることができます。(現在行われている、遺伝子組み換えの技術や遺伝子をターゲットにした治療などは、全て基礎研究での知識があってこそ可能です。)
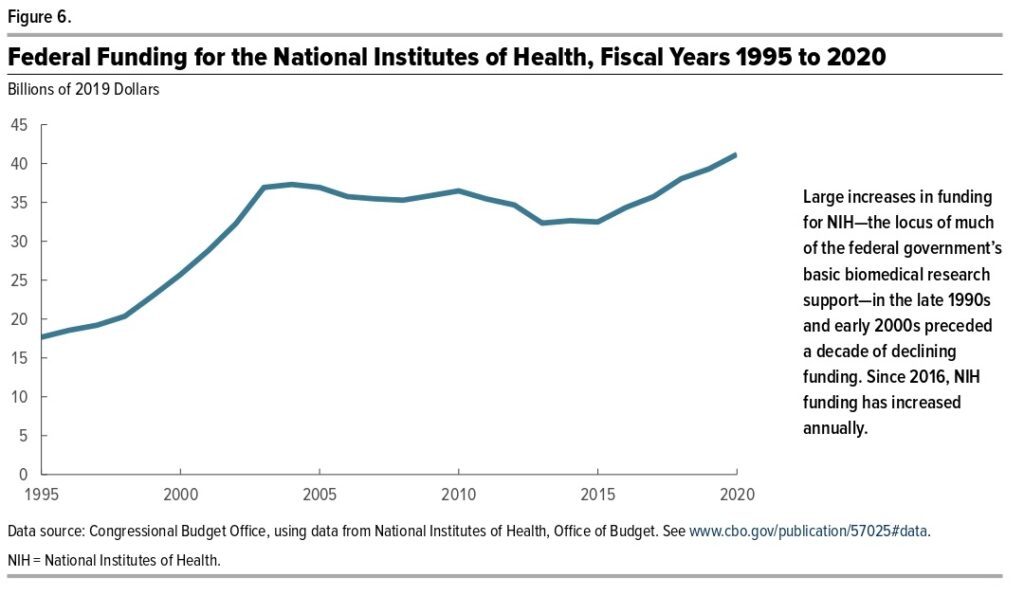
しかし、政府が資金提供すればするほど、政府にとっては支出が増えることを意味します。
製薬会社に対する税制優遇
政府は製薬会社が税制優遇を受けるための政策を打ち出すこともあります。
1983年に制定されたthe Orphan Drug Actという政策では、珍しい病気に対して研究開発を行う製薬会社に対して、税制優遇を施すことが定められています。
市場独占の法的容認
新薬は特許権(patent)という形で、市場を一定期間独占することが法的に認められています。他の製品と異なり、医薬品に関しては通常よりも長い年月この特許権が認められています。Royalty Pharma は特許権に基づくビジネスモデルを展開しており、またそれぞれの特許権は長期に渡り有効です。
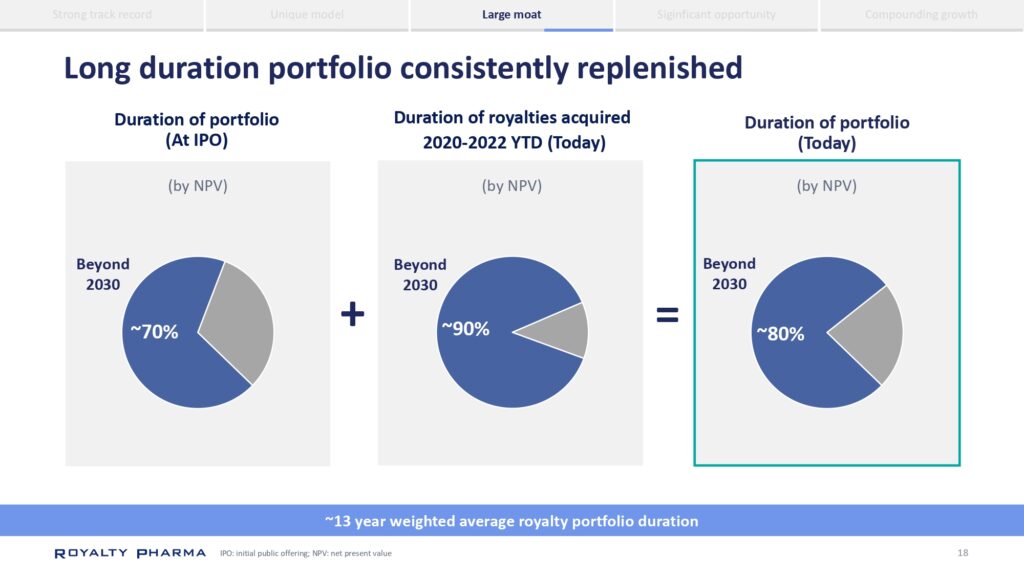
Royalty Pharma Investor Dayのプレゼンテーション資料からも分かる通り、平均して約13年ほど一つの特許権から収入を得ることができます。長期に渡り安定して収入を得ることができると言われるゆえんはここにあります。
ジェネリック医薬品の参入
ジェネリック医薬品とは、特許権が切れた薬の主成分を使い、他の製薬会社が同じ薬効を狙った薬を安い値段で製造、販売したものです。
コストが下がる分医療費を抑えることができるので、アメリカの政府をはじめ、日本でもジェネリック医薬品への切り替えが推奨されています。
(ただし、それが全て良いかについては、意見が分かれるところです。ジェネリック医薬品についてこの記事でも解説しています。)

さて、このジェネリック医薬品の参入というのは、ロイヤリティファーマにとってはマイナス影響となります。今まで売れていた薬が、競争が始まることで売れなくなる可能性が高いからです。
バイオシミラーについての扱い
まず、バイオシミラーについて簡単に解説します。
バイオシミラーというのは、生物製剤(生きた細胞に作らせたお薬)の代替薬です。いうなれば、我々が普段使いするような、昔からあるお薬だとジェネリック医薬品という立ち位置にある薬です。
ややこしいですよね。生物製剤の代替薬もジェネリック医薬品と言えばいいじゃないかと思われるかと思います。
しかし、それじゃダメな理由がちゃんとあるんです。
ジェネリック医薬品は、本家のお薬と有効成分は全く同じ分子を使っています。ロキソニンというお薬は、本家のロキソニンだとしても、ジェネリックのロキソプロフェンだとしても、有効成分のロキソプロフェンナトリウム水和物という成分は全く同じものです。
しかし、バイオシミラーの場合は、主成分として全く同じものを使うことができないのです。生物製剤を作るためには生きた細胞を使用する必要がありますが、実はどの細胞を使ったかに関して情報を公開しなくていいんです。すると競合他社が同じ生物製剤を作ろうと思ってもどの細胞を使って良いか分からず、結局全く同じ薬を作ることはほぼ不可能なのです。なので、バイオ”シミラー”(similar:似たもの)とされているのです。
バイオシミラーは、本家の生物製剤よりも研究開発費をかける必要がないため、より安価に製造することが可能です。薬のコストが下がることで結果として医療費を抑えることができるため、政府としてはバイオシミラーを推奨したい立場にあります。
では実際はバイオシミラーは医療費削減に貢献しているのでしょうか?
“Reserch and Development in the Pharmaceutical Industry”のデータによると、
2017年に販売された医薬品売上高 $125 billion (2017年のレート1ドル114円で、14兆2500億円)のうち、バイオシミラーに切り替え可能な医薬品の売り上げが $11 billion (1ドル114円で、1兆2540億円)でした。しかし、その $11 billion に対してバイオシミラーの売り上げはたった $0.9 billion (1ドル114円で、1026億円)でした。
なでこれほどまでにバイオシミラーへの切り替えが進んでいないのでしょうか?
やはりこれに関しても、医師、患者ともに、別の薬に変えることへの不安があるのです。
(ジェネリックに切り替えることへの不安な点について、以下の記事で解説してます。)

しかもジェネリックと違って、バイオシミラーへの切り替えは、有効成分が違うものへの切り替えを意味するので、切り替えのハードルはジェネリックよりも高いと思われます。
また、米国政府の方針として、生物製剤は、従来の有機化学で作られる小分子の医薬品よりも、特許権が長期間に設定されています(生物製剤は12年に対して、小分子の医薬品は約5年)。これは生物製剤を開発することの難しさを物語っています。
例えばRoyalty Pharma が特許権を持つ Imbruvica という慢性リンパ性白血病の治療薬においてもそうです。
同薬剤は生物製剤(バイオ製剤)で、もともとRoyalty Pharma のロイヤリティは2027年から2029年の間に消失すると予想されていました。しかし、2021年度の年間報告書 (Annual report) では2027年から2032年の間と期間が延長されています。
Royalty Pharma 2021 10-K Annual Reportこの理由としては、Imbruvicaのバイオシミラーを製造しようとしていた会社を、Abbvie とジョンソンエンドジョンソンが訴え、それが受理されたからです。(理由としては特許権の侵害ということです。)
生物製剤(バイオ製剤)を製造するには数々の技術が必要で、それぞれに特許権が絡んでいます。そのため、バイオシミラーを製造しようとしても、特許権を侵害せずに製造することが難しく、参入障壁が非常に高いのです。
この件に関して、Royalty Pharma にとっては好都合で、Imbruvica からのロイヤリティ収入を受け取る期間が延びる可能性を示唆しています。
政策(医薬品の値段や臨床試験の基準の制定)
政府は薬の値段や、臨床試験の基準に介入することでも、薬の供給に影響を及ぼすことができます。臨床試験の合格基準を緩和すれば、その分市場に新薬が出回る可能性が増えます(例えばアルツハイマー病の治療薬など)。逆に、臨床試験の合格基準を厳しくすれば、新薬が市場に回る可能性は低くなります。
次のページでRoyalty Pharma が受ける恩恵について解説です。